การกำกับดูแลก่อนออกสู่ตลาด เครื่องมือแพทย์ที่มีกำลัง (Active Medical Device)
การกำกับดูแลก่อนออกสู่ตลาด เครื่องมือแพทย์ที่มีกำลัง (Active Medical Device)
การแจ้งรายการละเอียดเครื่องมือแพทย์
เครื่องมือแพทย์ที่ต้องแจ้งรายการละเอียด ได้แก่ เครื่องมือแพทย์ที่มีกำลัง (active medical device) ประเภทความเสี่ยง 2-3
กฎหมายที่เกี่ยวข้อง
- กฎกระทรวง การแจ้งรายการละเอียดและการออกใบรับแจ้งรายการละเอียดผลิตหรือนำเข้าเครื่องมือแพทย์ พ.ศ. 2563
- ประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง กำหนดข้อมูล เอกสาร หรือหลักฐานที่ไม่ต้องแจ้งตามกฎกระทรวงว่าด้วยเรื่องการอนุญาตและการออกใบอนุญาตผลิตหรือนำเข้าเครื่องมือแพทย์ และการแจ้งรายการละเอียดและการออกใบรับแจ้งรายการละเอียดผลิตหรือนำเข้าเครื่องมือแพทย์ พ.ศ. 2567
- ประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง รายชื่อหน่วยงานต่างประเทศที่อย.ยอมรับการตรวจสอบหรือการรับรองเครื่องมือแพทย์หรือสถานประกอบการด้านเครื่องมือแพทย์ พ.ศ. 2567
การยื่นเอกสารขึ้นทะเบียนผลิตภัณฑ์เครื่องมือแพทย์
จัดเตรียมเอกสารเพื่อใช้ยื่นคำขอขึ้นทะเบียนเครื่องมือแพทย์ รูปแบบ Common Submission Dossier Template (CSDT)
ขั้นตอนการยื่นคำขอขึ้นทะเบียนเครื่องมือแพทย์เพื่อผลิตหรือนำเข้า
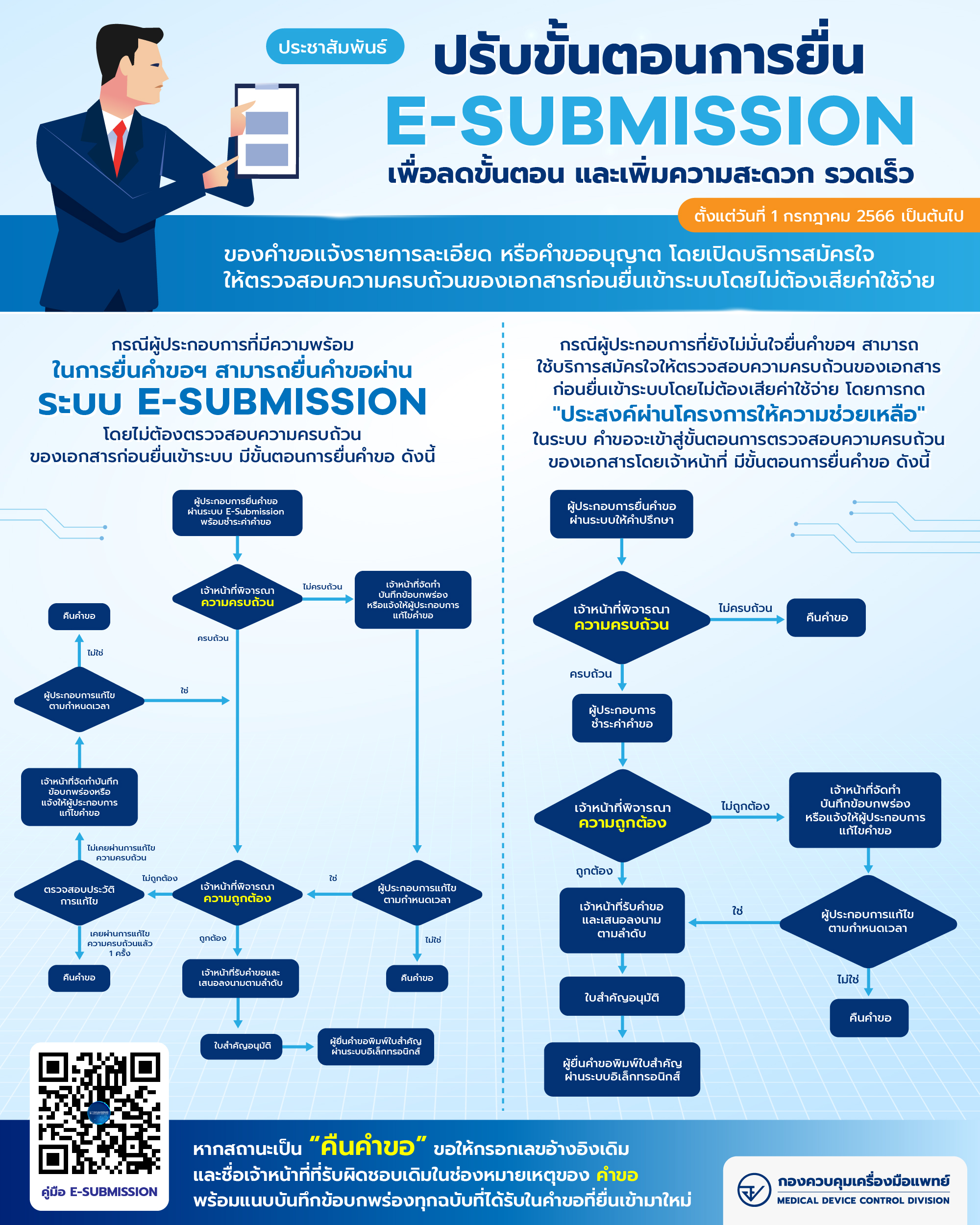
การประเมินเอกสาร CSDT
การประเมินเอกสารแบบเต็มรูปแบบ (Full evaluation)
Reliance Program Device Registration กรณีเครื่องมือแพทย์ได้ขึ้นทะเบียนที่ประเทศสิงคโปร์และ Registrant ที่สิงคโปร์สามารถออกเอกสาร consent form ให้ อย สามารถเข้าถึง evaluation report ที่ออกโดย HSA สิงคโปร์ได้ ซึ่งจะไม่ต้องส่งเอกสารให้ผู้เชี่ยวชาญภายนอกประเมิน
▶ข้อมูลเพิ่มเติมเกี่ยวกับการขึ้นทะเบียนเครื่องมือแพทย์แบบ Reliance
การประเมินเอกสารแบบย่อ (Abridged evaluation) กรณีเครื่องมือแพทย์มีประวัติการขึ้นทะเบียนหรือได้รับอนุญาตจากหน่วยงานที่ อย. รับรอง (reference regulatory agency) ใน Big 5 Countries (EU, USA, Canada, Australia, Japan) อย่างน้อย 1 ปีขึ้นไป ผู้ยื่นคำขอขึ้นทะเบียนผลิตภัณฑ์สามารถใช้สิทธ์ในการประเมินเอกสารแบบย่อ (Abrided evaluation) ซึ่งเป็นช่องทางที่ช่วยอำนวยความสะดวกในการขึ้นทะเบียนเครื่องมือแพทย์ ไม่ต้องประเมินเอกสารทางวิชาการซํ้าซ้อน ลดระยะเวลาลดค่าใช้จ่ายลดภาระงานของเจ้าหน้าที่และผู้ประกอบการ และประชาชนเข้าถึงเครื่องมือแพทย์ที่มีคุณภาพและมาตรฐานได้อย่างรวดเร็ว
▶ข้อมูลเพิ่มเติมเกี่ยวกับช่องการการยื่นเอกสารขึ้นทะเบียนเครื่องมือแพทย์

ข้อมูลอื่นๆ ที่เกี่ยวข้องกับเครื่องมือแพทย์ที่มีกำลัง