
ช่องทางการยื่นเอกสารสำหรับขึ้นทะเบียนเครื่องมือแพทย์ที่ต้องขอใบอนุญาตและใบรับแจ้งรายการละเอียด
แบ่งช่องทางการยื่นเอกสารเป็น 2 รูปแบบ ดังนี้ 1.การยื่นเอกสารแบบเต็มรูปแบบ (Full pathway) 2.การยื่นเอกสารแบบย่อ (Abridged pathway) ...
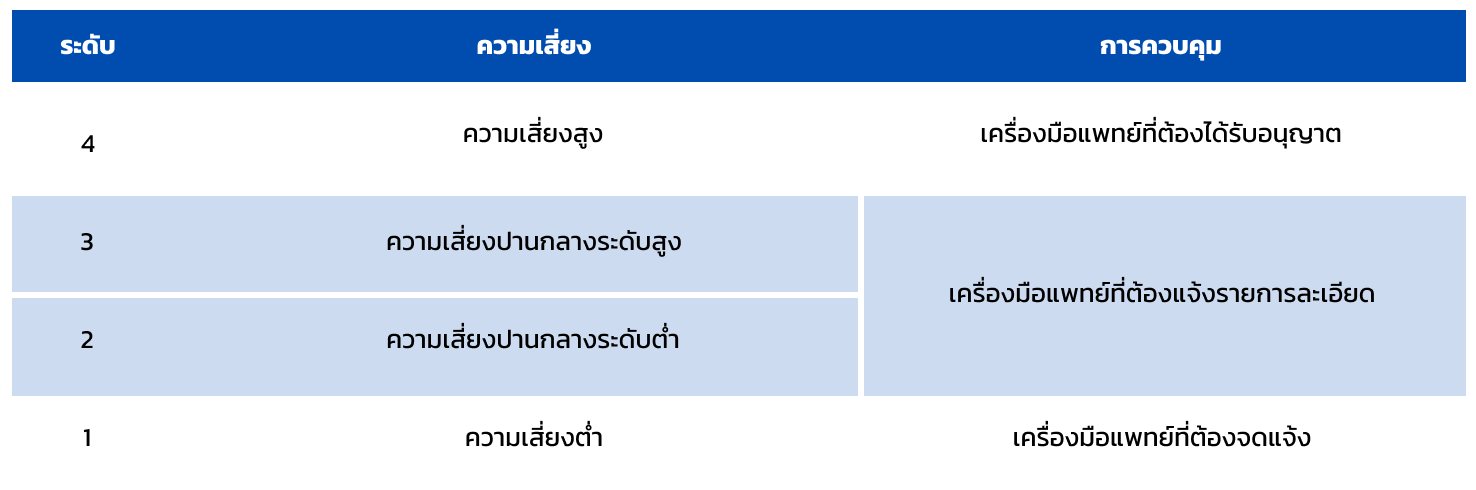
ผู้ผลิตเครื่องมือแพทย์ หรือผู้นำเข้าเครื่องมือแพทย์เพื่อขายในประเทศไทยจะต้องขึ้นทะเบียนผลิต หรือนำเข้าเครื่องมือแพทย์กับสำนักงานอาหารและยาให้เสร็จสิ้นก่อน ปัจจุบันประเทศไทยมีการควบคุมเครื่องมือแพทย์ตามระดับความเสี่ยงของเครื่องมือแพทย์ตามประกาศกระทรวงสาธารณสุข เรื่อง การจัดประเภทเครื่องมือแพทย์ตามระดับความเสี่ยง พ.ศ. 2562 ดังนี้
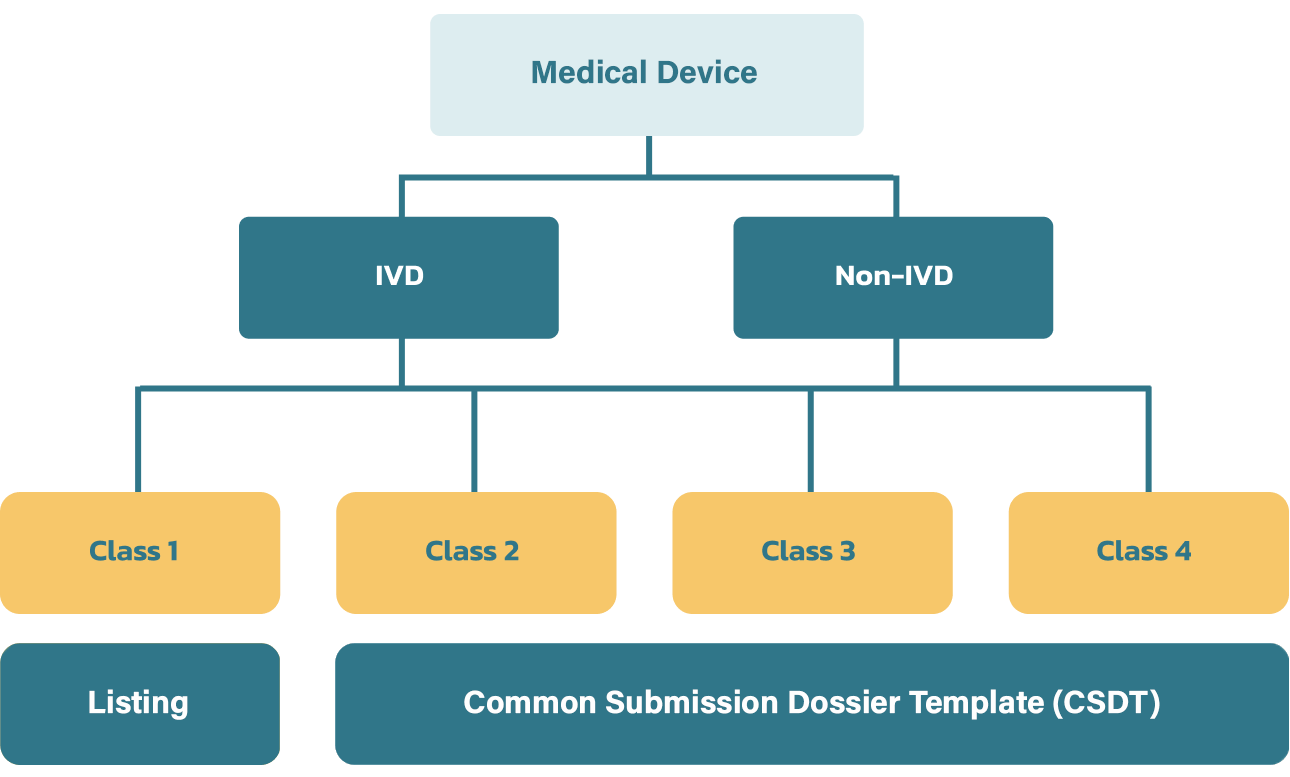
การจัดประเภทเครื่องมือแพทย์ตามระดับความเสี่ยง
สามารถศึกษารายละเอียดการจัดประเภทเครื่องมือแพทย์ได้ตามประกาศกระทรวงสาธารณสุขเรื่องการจัดเครื่องมือแพทย์ตามความเสี่ยง พ.ศ. 2562 และสามารถศึกษาตัวอย่างประเภทของเครื่องมือแพทย์ตามความเสี่ยงเพิ่มเติมได้ที่คู่มือหลักเกณฑ์การจัดประเภทเครื่องมือแพทย์ตามความเสี่ยง เพื่อให้สามารถขออนุญาตเครื่องมือแพทย์ได้ถูกต้องตามประเภทเครื่องมือแพทย์
หากท่านต้องการขึ้นทะเบียนเครื่องมือแพทย์ ท่านจะต้องทำการจัดประเภทความเสี่ยงของผลิตภัณฑ์ของท่านก่อน (Risk classification) และการรวมกลุ่มของเครื่องมือแพทย์ (grouping) เนื่องจากทั้งสองปัจจัยมีผลต่อการยื่นคำขอ และเอกสารประกอบการยื่นคำขอ โดยสรุปได้ดังตาราง
ประเภทความเสี่ยง เครื่องมือแพทย์ | ระดับความเสี่ยง | กลุ่มเครื่องมือแพทย์ | เอกสารประกอบ การยื่นคำขอ |
เครื่องมือแพทย์ประเภทที่ 1 และเครื่องมือแพทย์สำหรับสัตว์ | ความเสี่ยงต่ำ | กลุ่มเครื่องมือแพทย์หรือเครื่องมือแพทย์ที่ผู้ผลิตหรือผู้นำเข้าต้องจดแจ้ง (Listing medical device) | ตามกฎกระทรวงการจดแจ้งและการออกใบรับจดแจ้งผลิตหรือนำเข้าเครื่องมือแพทย์ พ.ศ. 2563 |
เครื่องมือแพทย์ประเภทที่ 2,3 | ความเสี่ยงปานกลาง | กลุ่มเครื่องมือแพทย์หรือเครื่องมือแพทย์ที่ผู้ผลิตหรือผู้นำเข้าต้องแจ้งรายการละเอียด (ฉบับที่ 1),(ฉบับที่ 2) | ตามกฎกระทรวงการแจ้งรายการละเอียดและการการออกใบรับแจ้งรายการละเอียดผลิตหรือนำเข้า |
เครื่องมือแพทย์ประเภทที่ 4 | ความเสี่ยงสูง | กลุ่มเครื่องมือแพทย์หรือเครื่องมือแพทย์ที่ผู้ผลิตหรือผู้นำเข้าต้องได้รับอนุญาต | ตามกฎกระทรวงการขออนุญาตและการออกใบอนุญาตผลิตหรือนำเข้าเครื่องมือแพทย์ พ.ศ. 2563 |
การจัดกลุ่มเครื่องมือแพทย์
สามารถศึกษารายละเอียดการจัดกลุ่มเครื่องมือแพทย์ได้ ตามประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง หลักเกณฑ์ในการจัดกลุ่มเครื่องมือแพทย์
**กรณีต้องการหนังสือรับรองการจัดประเภทเครื่องมือแพทย์ตามความเสี่ยงและการจัดกลุ่มเครื่องมือแพทย์
สามารถยื่น ขอหนังสือรับรองการจัดประเภทเครื่องมือแพทย์ตามความเสี่ยงและการจัดกลุ่มเครื่องมือแพทย์
หรือ
โปรแกรมเบื้องต้นสำหรับการจัดประเภทเครื่องมือแพทย์ตามความเสี่ยงเพื่อตรวจสอบประเภทความเสี่ยง ด้วยตนเอง
(ใช้เป็นข้อมูลเบื้องต้นเท่านั้น ไม่สามารถใช้เป็นเอกสารยืนยัน หรืออ้างอิงในการขึ้นทะเบียนได้)
เครื่องมือแพทย์ที่มีประกาศฯ เฉพาะ
เครื่องมือแพทย์ที่มีประกาศกระทรวงสาธารณสุขฯ เฉพาะ ที่ต้องยื่นคำขอขึ้นทะเบียนผลิตภัณฑ์แบบ Full CSDT (ตาม กฎกระทรวงการแจ้งรายการละเอียดและการการออกใบรับแจ้งรายการละเอียดผลิตหรือนำเข้า เครื่องมือแพทย์ พ.ศ. 2563 และ กฎกระทรวงการขออนุญาตและการออกใบอนุญาตผลิตหรือนำเข้าเครื่องมือแพทย์ พ.ศ. 2563) ได้แก่
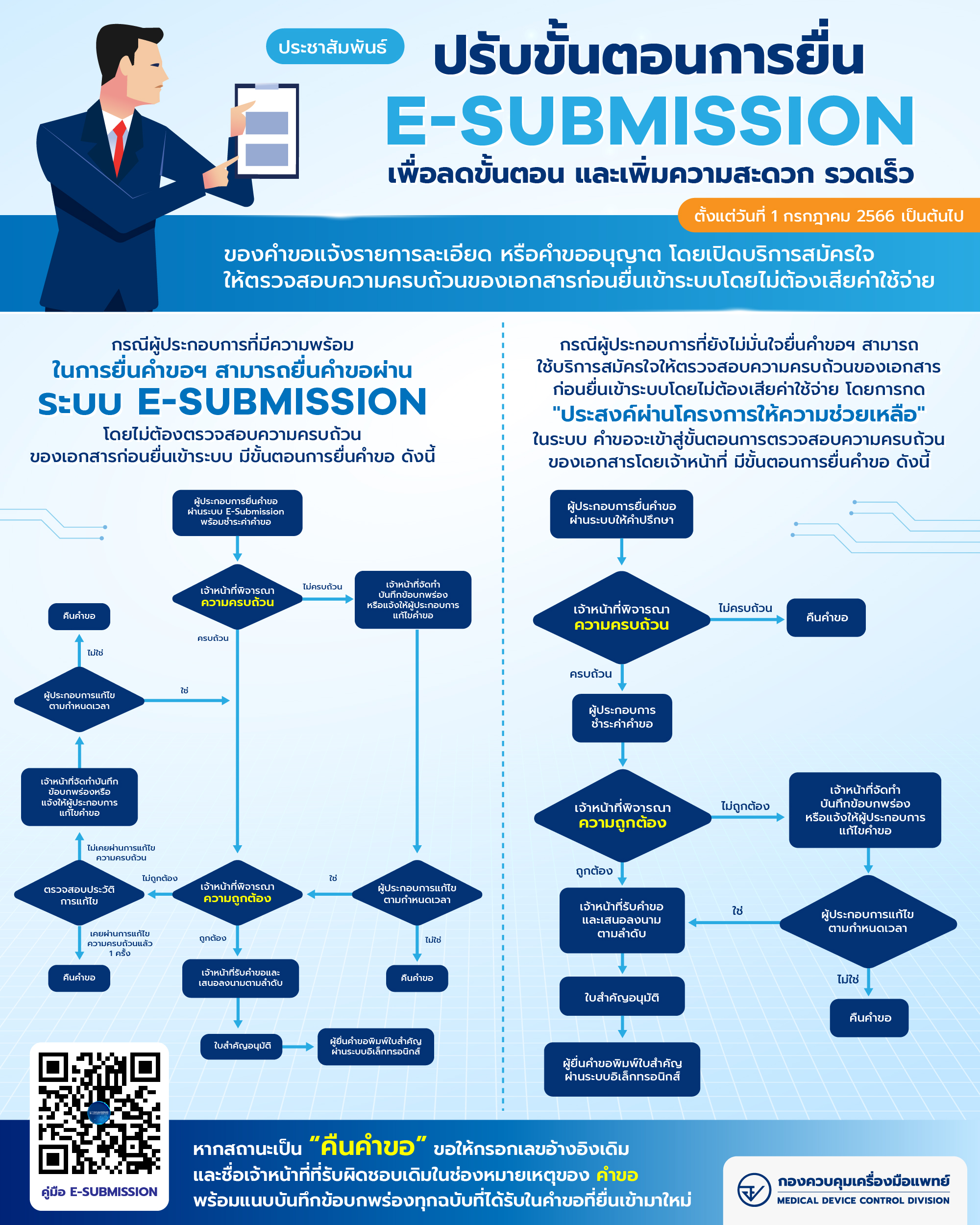
ขั้นตอนการขึ้นทะเบียนผลิตภัณฑ์

เลือกหัวข้อที่ท่านต้องการ Subscribe